Entre espoir et patience
Le 6 mars 2026 marque un tournant historique pour la neurologie : le Japon est devenu le premier pays au monde à autoriser la commercialisation d’une thérapie à base de cellules souches pour traiter la maladie de Parkinson. Baptisé Amchepry (développé par Sumitomo Pharma et l’Université de Kyoto), ce traitement promet de transformer la gestion de la maladie.
Que sont ces cellules « reprogrammées » ?
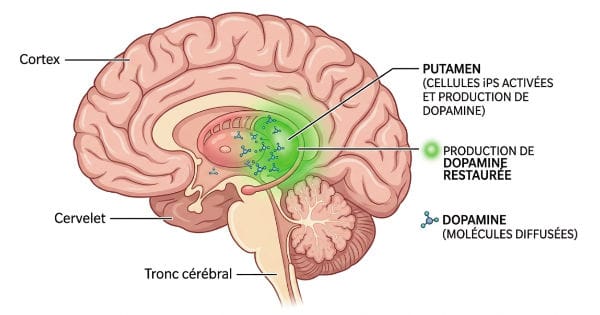
Fonction dopaminergique restaurée dans le Putamen après transplantation de cellules iPS
L'essai clinique : 6 ou 7 patients ?
Une confusion persiste souvent sur les chiffres. Voici la réalité de l’étude publiée dans Nature (2026) :
- 7 patients ont été opérés : C’est le nombre total de participants ayant reçu la greffe dans l’essai de l’Université de Kyoto.
- Le focus sur 6 patients : Si vous lisez parfois le chiffre « 6 », c’est parce que les données d’efficacité à long terme les plus homogènes et complètes concernent 6 des 7 participants. L’un des patients a pu présenter un profil clinique ou une réponse statistique légèrement différente, amenant les chercheurs à détailler les résultats sur ce groupe de 6 pour plus de précision scientifique.
- Résultats : Sur ces participants, 4 ont montré une amélioration spectaculaire de leur motricité, réduisant significativement leurs périodes de « blocage » (phases OFF).
Le « modèle japonais » : Pourquoi eux et pas nous ?
Le Japon dispose d’une législation unique (la loi PMD Act) qui permet une approbation conditionnelle.
- Le principe : Si la sécurité est prouvée sur un petit groupe et que le traitement semble fonctionner, il peut être vendu immédiatement.
- La contrepartie : Le fabricant a 7 ans pour prouver l’efficacité réelle sur un plus grand nombre de patients.
- Ailleurs : En Europe (EMA) et aux États-Unis (FDA), les autorités exigent des preuves massives (Phase 3 avec groupe placebo) avant toute mise sur le marché, ce qui explique pourquoi les patients occidentaux devront encore patienter plusieurs
années.
Pourquoi ce n'est pas (encore) un remède miracle ?
La Michael J. Fox Foundation (MJFF) reste prudente : ce traitement est une thérapie de remplacement, pas une guérison.
- Une rustine de luxe : On remplace les neurones morts pour restaurer la dopamine, mais on ne stoppe pas la cause de la maladie. La dégénérescence peut continuer ailleurs.
- Symptômes ignorés : La greffe aide pour les tremblements et la rigidité, mais agit peu sur la dépression, les troubles du sommeil ou la mémoire.
- Complexité : L’implantation nécessite une neurochirurgie lourde et précise dans le putamen (une zone profonde du cerveau).
En somme, l’arrivée d’Amchepry sur le marché japonais est une preuve de concept historique qui valide des décennies de recherche sur les cellules iPS. Si cette avancée offre une alternative biologique prometteuse aux traitements chimiques, elle reste une étape : un outil pour mieux vivre avec la maladie, plutôt qu’une baguette magique pour l’effacer.
Pour les patients du reste du monde, le défi sera désormais de transformer cet essai en un standard de soin global, accessible et validé par des études à plus large échelle.
Sources et références pour aller plus loin
- Nature (06/03/2026) : « Trial of iPSC-derived dopamine progenitors in Parkinson’s disease«
(Article scientifique sur les résultats de l’essai de
Kyoto). - NHK World (06/03/2026) : « Japan approves world’s first iPS cell therapy for Parkinson’s » (Article de presse annonçant l’approbation).
- Michael J. Fox Foundation (MJFF) : « Stem Cell and Cell-Based Therapies for Parkinson’s: What to Know Now » (Guide de référence pour les patients).
- ScienceDirect / Parkinsonism & Related Disorders (2025) : « Preclinical safety and efficacy profile of clinical-grade human induced pluripotent stem cell-derived dopamine progenitors (Amchepry) » (Étude technique sur la sécurité des cellules).
- Center for iPS Cell Research and Application (CiRA), Université de Kyoto : Le centre du Prix Nobel Shinya Yamanaka (créateur des iPS). Informations détaillées sur la fabrication des cellules. (En anglais).
- Base de données ClinicalTrials.gov (NCT03655639) : Les détails techniques du protocole initial de l’essai de Kyoto.
- Informations sur l’approbation par la PMDA (Japon) : (Généralement disponible sur le site de Sumitomo Pharma après l’annonce officielle).
